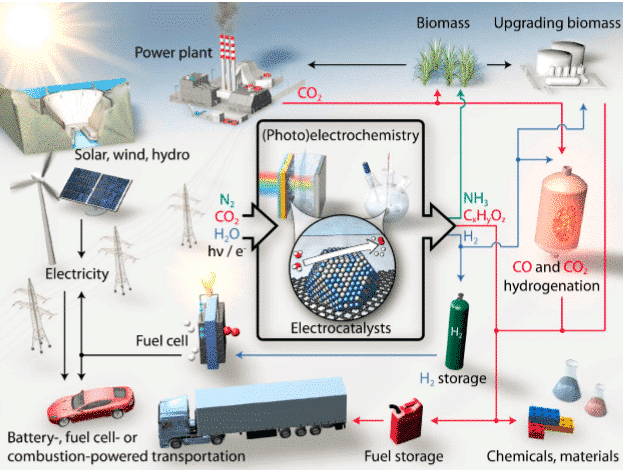
電催化反應(yīng)技術(shù)是推動(dòng)這些能量轉(zhuǎn)換和環(huán)境凈化途徑的關(guān)鍵方法之一。
近年來(lái),隨著社會(huì)的發(fā)展和人類(lèi)的進(jìn)步,日益嚴(yán)重的能源和環(huán)境問(wèn)題已成為世界性難題,亟待解決。人們致力于新能源的有效利用和環(huán)境的長(zhǎng)期凈化方法。目前促進(jìn)能源轉(zhuǎn)化和環(huán)境凈化的有效研究方法涉及燃料電池開(kāi)發(fā)、制氫、CO2資源化、廢氣有機(jī)催化轉(zhuǎn)化等多個(gè)方向。電化學(xué)測(cè)試方法作為理論指導(dǎo)為電催化劑性能的發(fā)展提供了合理的解釋手段。本文總結(jié)了幾種電化學(xué)反應(yīng)中常用的電化學(xué)測(cè)試方法。
圖1 可持續(xù)能量轉(zhuǎn)換電催化過(guò)程
1.循環(huán)伏安法
循環(huán)伏安法 (CV) 是評(píng)估未知電化學(xué)系統(tǒng)最常用的研究方法。主要是通過(guò)控制不同速率的電極電位,隨時(shí)間用三角波形掃描一次或多次獲得。電流-電位曲線 (iE)。不同的還原和氧化反應(yīng)可以在不同電位范圍的電極上交替發(fā)生??筛鶕?jù)曲線的形狀判斷電極反應(yīng)的可逆性;反應(yīng)物的吸附和解吸峰可用于根據(jù)特定電位范圍評(píng)估電催化劑。催化活性區(qū)域還可用于獲得有關(guān)復(fù)雜電極反應(yīng)的有用信息。
圖 1.1 掃描電流電位響應(yīng)曲線
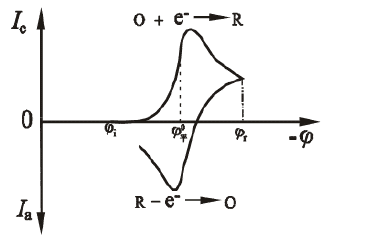
如圖1.1所示,前半部分的電位向陰極掃描,電活性物質(zhì)在電極上被還原,產(chǎn)生還原波。當(dāng)后半部分的電位向陽(yáng)極掃描時(shí),還原產(chǎn)物在電極上再次被氧化,產(chǎn)生氧化波。循環(huán)伏安 iE 曲線的兩個(gè)有用參數(shù)是峰值電流比 ipa/ipc 和峰值電位差 Epa-Epc。對(duì)于穩(wěn)定產(chǎn)物的能斯特波,峰值電流比 ipa/ipc = 1,與掃描速度、擴(kuò)散系數(shù)和換向電位無(wú)關(guān)。當(dāng)陰極掃描停止時(shí),電流降為0,然后反向掃描。得到的iE曲線與陰極曲線完全一樣,只是畫(huà)在I坐標(biāo)和E坐標(biāo)的相反方向上。 ipa/ipc 比值偏離 1,表明電極過(guò)程不是一個(gè)完全可逆的反應(yīng)過(guò)程,涉及均相動(dòng)力學(xué)或其他復(fù)雜性。反應(yīng)峰高和峰面積可用于估計(jì)系統(tǒng)參數(shù),例如電活性物質(zhì)的濃度或偶合均相反應(yīng)的速度常數(shù)。然而,CV曲線并不是一種理想的定量方法,其強(qiáng)大的用途更多在于其定性半定量的判斷能力。
2.脈沖伏安法
脈沖伏安法是一種基于極譜電極行為的電化學(xué)測(cè)量方法。用于研究各種介質(zhì)中的氧化還原過(guò)程、表面材料對(duì)催化劑材料的吸附以及化學(xué)修飾電極表面的電子轉(zhuǎn)移機(jī)理。檢測(cè)特別有效。根據(jù)掃描電壓的方式,脈沖伏安法包括步進(jìn)伏安法、常規(guī)脈沖伏安法、差分脈沖伏安法和方波伏安法。其中,步進(jìn)伏安法類(lèi)似于電位掃描法,大多數(shù)系統(tǒng)對(duì)更高分辨率(ΔE < 5 mV)步進(jìn)伏安的響應(yīng)與相同掃描速度的線性掃描實(shí)驗(yàn)結(jié)果非常相似。
3. 電化學(xué)阻抗譜
電化學(xué)阻抗譜是向電化學(xué)系統(tǒng)施加擾動(dòng)的電信號(hào)。與線性掃描法不同的是,電化學(xué)系統(tǒng)遠(yuǎn)離平衡態(tài),然后觀察系統(tǒng)的響應(yīng),通過(guò)響應(yīng)電信號(hào)分析系統(tǒng)的電化學(xué)性質(zhì)。電化學(xué)阻抗譜常用于分析、評(píng)價(jià)PEM燃料電池中的ORR反應(yīng),表征催化劑材料表面的擴(kuò)散損失,估算歐姆電阻,以及電荷轉(zhuǎn)移阻抗和雙層電容的特性來(lái)評(píng)價(jià)和優(yōu)化膜電極組件。
阻抗譜通常以波特圖和奈奎斯特圖的形式繪制。在波德圖中,阻抗的幅度和相位被繪制為頻率的函數(shù);在奈奎斯特圖中,阻抗的虛部繪制在相對(duì)于實(shí)部的每個(gè)頻率點(diǎn)處。高頻電弧反映了催化劑層的雙層電容、有效電荷轉(zhuǎn)移阻抗和歐姆電阻的組合,反映了質(zhì)量轉(zhuǎn)移產(chǎn)生的阻抗。對(duì)于給定的系統(tǒng),這兩個(gè)區(qū)域有時(shí)沒(méi)有很好地定義。
圖 3.1 電化學(xué)系統(tǒng)的阻抗譜
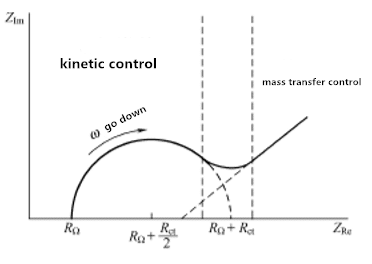
圖 3.1 顯示了動(dòng)力學(xué)控制和傳質(zhì)控制的極端特性。然而,對(duì)于任何給定的系統(tǒng),這兩個(gè)區(qū)域可能都沒(méi)有很好地定義。決定因素是電荷轉(zhuǎn)移電阻和傳輸阻抗之間的關(guān)系。如果化學(xué)系統(tǒng)的動(dòng)力學(xué)很慢,它會(huì)顯示出很大的 Rct,這似乎具有非常有限的頻率區(qū)域。當(dāng)系統(tǒng)是動(dòng)態(tài)的時(shí),材料傳遞總是起主導(dǎo)作用,半圓形區(qū)域很難定義。
4.計(jì)時(shí)電流法
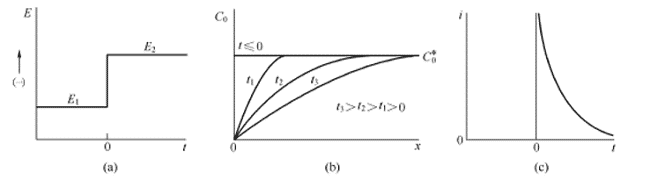
計(jì)時(shí)電流法是一種瞬態(tài)控制方法,可用于評(píng)價(jià)催化劑表面的吸附和擴(kuò)散。計(jì)時(shí)電流曲線是通過(guò)對(duì)電化學(xué)系統(tǒng)施加電位階躍來(lái)測(cè)量電流響應(yīng)信號(hào)隨時(shí)間的變化而獲得的。當(dāng)給定電位階躍時(shí),基本波形如圖 4.1(a) 所示,用電活性材料分析固體電極的表面。施加電位階躍后,電極表面附近的電活性物質(zhì)首先被還原為穩(wěn)定的陰離子自由基,這需要大電流,因?yàn)樵撨^(guò)程立即發(fā)生在階躍瞬間。此后流動(dòng)的電流用于維持電極表面活性材料完全還原的條件。初始還原導(dǎo)致電極表面和本體溶液之間產(chǎn)生濃度梯度(即濃度),因此活性材料開(kāi)始不斷地向表面擴(kuò)散并擴(kuò)散到電極。表面的活性物質(zhì)立即完全還原。擴(kuò)散流,即電流,與電極表面的濃度梯度成正比。但需要注意的是,隨著反應(yīng)的進(jìn)行,本體溶液中的活性物質(zhì)不斷向電極表面擴(kuò)散,導(dǎo)致濃度梯度區(qū)逐漸向本體溶液延伸,固體電極的表面濃度梯度逐漸增大。變?。ê谋M),電流逐漸變化。小的。濃度分布和電流與時(shí)間的關(guān)系如圖 4.1(b) 和圖 4.1(c) 所示。
圖 4.1 (a) 階躍實(shí)驗(yàn)波形,反應(yīng)物 O 在電位 E1 不反應(yīng),在 E2 處以擴(kuò)散極限速度還原; (b) 不同時(shí)間的濃度分布; (c) 電流與時(shí)間曲線
5.轉(zhuǎn)盤(pán)電極技術(shù)
旋轉(zhuǎn)盤(pán)電極(RDE)技術(shù)在研究催化劑表面的耦合均相反應(yīng)方面非常有用,使催化劑表面的電化學(xué)反應(yīng)在相對(duì)穩(wěn)定的條件下進(jìn)行。 RDE可以控制擴(kuò)散較慢的物質(zhì),例如容易擴(kuò)散到溶液中的氣體,減少擴(kuò)散層對(duì)電流密度分布的影響。從而得到穩(wěn)定的電流密度,處于近似穩(wěn)態(tài),有利于電化學(xué)分析過(guò)程; RDE可以通過(guò)調(diào)節(jié)轉(zhuǎn)速來(lái)控制電解液到達(dá)電極表面的速度,測(cè)量不同轉(zhuǎn)速下電催化反應(yīng)過(guò)程的參數(shù)。分析。
隨著人類(lèi)對(duì)開(kāi)發(fā)用于清潔能源轉(zhuǎn)換的先進(jìn)電催化劑越來(lái)越感興趣,除了強(qiáng)調(diào)使用一些基本方法來(lái)表征電催化反應(yīng)外,還需要進(jìn)一步檢查每個(gè)反應(yīng)的基本步驟,以確定所涉及的關(guān)鍵組合中間體、中間體的表面以及每個(gè)基本反應(yīng)步驟的能量。電化學(xué)方法的研究仍然需要關(guān)于電極-電解質(zhì)界面的許多迄今為止未知的細(xì)節(jié),例如質(zhì)子/電子轉(zhuǎn)移關(guān)鍵基本步驟所涉及的動(dòng)力學(xué)和反應(yīng)勢(shì)壘;靠近溶劑、陽(yáng)離子和反應(yīng)界面。陰離子的原子、分子水平狀態(tài)描述;而在整個(gè)電化學(xué)反應(yīng)過(guò)程中更快、更高效的實(shí)時(shí)信號(hào)采集方法仍處于電催化反應(yīng)的前沿??傊钊胙芯侩娀瘜W(xué)表征方法為開(kāi)發(fā)新型高效催化劑體系提供了指導(dǎo)策略。